-
Главная

-
Лечение онкологии

- Рак груди
Последнее обновление: 16 марта 2024 г.
Эффективные стратегии борьбы с раком груди: обзор современных подходов
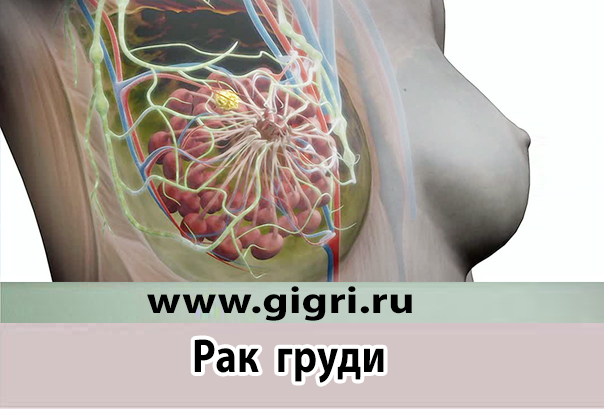
Функция груди: выработка грудного молока. Задача женской груди производить грудное молоко после рождения и во время грудного вскармливания ребенка и таким образом питать новорожденного. Грудное молоко вырабатывается в железистой ткани – точнее, в молочных железах, которые расположены в железистых дольках. По молочным протокам она попадает в так называемые молочные мешочки, которые расположены непосредственно перед соском. Здесь изначально собирается грудное молоко. Когда ребенок сосет грудь, она в конечном итоге вытекает через сосок.
Что такое рак молочной железы? Рак молочной железы – это заболевание, при котором в молочной железе растет злокачественная инвазивная опухоль. Рак молочной железы – это рак, возникающий в молочной железе. Когда клетки молочной железы начинают бесконтрольно расти, в молочной железе развиваетсопухоль. Если эта опухоль молочной железы деструктивно (инвазивно) прорастает в окружающую ткань и тем самым повреждает ее, ее считают злокачественной – это рак молочной железы.
Почему развивается рак молочной железы? Точные причины рака молочной железы часто неясны. Почему развивается рак молочной железы, для многих женщин в конечном итоге неясно. Генные изменения, которые способствуют или вызывают рак молочной железы, обычно возникают случайно, когда клетки молочной железы делятся неправильно. Но внешние воздействия также могут привести к необратимому повреждению генетического материала и, следовательно, к генетическим изменениям. Важно знать: если поврежденная клетка не умирает, изменения гена сохраняются навсегда. Поэтому они могут накапливаться в течение жизни. Существуют также генетические изменения, которые увеличивают риск рака молочной железы, который вы можете унаследовать от своих родителей. Такое наследственное генетическое изменение присутствует в каждой клетке тела пострадавшего. Однако существуют факторы, повышающие риск рака молочной железы. Эксперты подозревают, что несколько таких факторов риска могут вместе вызвать рак молочной железы, и не на все из них можно повлиять. Факторами риска, на которые невозможно повлиять, являются:
- старший возраст
- наследственная предрасположенность
- плотная ткань молочной железы
- определенные изменения в ткани молочной железы
- предыдущая лучевая терапия грудной клетки
- сахарный диабет 2 типа
- гормональные факторы
Факторами риска, на которые можно повлиять, являются:
- потребление алкоголя
- дым
- недостаток упражнений
- нездоровое питание
- отсутствие или короткие периоды грудного вскармливания
- гормональные контрацептивы (таблетки и спираль)
- лишний вес после менопаузы
- заместительная гормональная терапия после менопаузы.
Рак молочной железы: диагностика
Если женщина замечает изменения в молочных железах или раннее обследование выявляет отклонения от нормы, врач сначала изучает подробный анамнез (анамнез). Затем пальпируют грудь и подмышки пострадавшей женщины. После этого обычно проводится маммография, а в некоторых случаях также проводится ультразвуковое исследование или магнитно-резонансная томография (МРТ). Если эти обследования выявляют какие-либо отклонения, врач возьмет образец ткани из подозрительного участка молочной железы. Эксперты называют это биопсией. Только исследовав удаленную ткань под микроскопом, можно определить, действительно ли это рак. Если подозрение на рак подтвердится, в зависимости от случая могут потребоваться дальнейшие обследования.
Маммография
Маммография может использовать рентгеновские лучи, чтобы сделать видимыми даже самые незначительные изменения в груди. Помимо небольших опухолей, которые еще невозможно прощупать, можно обнаружить и небольшие кальцинаты, так называемые микрокальцинаты. Микрокальцификация может указывать на предвестник рака, а также на сам рак. Если маммография выявляет отклонения от нормы, необходимы дальнейшие обследования.
Как и любое рентгеновское исследование, маммография также предполагает определенное радиационное воздействие. Сегодня маммографические аппараты сконструированы таким образом, чтобы пострадавшие женщины подвергались как можно меньшему воздействию радиации.
УЗИ молочной железы
В принципе, маммография – лучший метод выявления изменений в молочной железе. В определенных случаях может оказаться полезным и ультразвуковое исследование . Иногда врачи не могут с уверенностью оценить рентгеновские снимки маммографии. Затем назначают дополнительное ультразвуковое исследование молочных желез. Даже женщинам до 40 лет в первую очередь проводится ультразвуковое исследование при наличии каких-либо отклонений в молочной железе. УЗИ также является неотъемлемой частью последующих обследований. Если у женщин есть проблемы с грудью, их сначала обследуют с помощью УЗИ.
Биопсия
Если маммография или ультразвуковое исследование выявляют подозрительные результаты, врач берет образец ткани из подозрительного участка молочной железы. Это единственный способ окончательно определить, действительно ли это рак. Затем образец исследуют под микроскопом в лаборатории. В большинстве случаев образец ткани можно взять с помощью полой иглы. Эксперты называют это «минимально инвазивной процедурой». Процедура обычно проводится под местной анестезией и в амбулаторных условиях. Для взятия образца ткани редко требуется серьезная операция.
Если в лаборатории выясняется, что у женщины действительно рак молочной железы, образцы тканей исследуются дополнительно. Таким образом, можно оценить дальнейшее течение заболевания и спланировать лечение. Специалисты стараются узнать как можно больше об особенностях рака:
Какой тип рака у женщины? Из каких клеток возникает рак? Как быстро растет рак?
Исследование под микроскопом также позволяет выяснить, насколько раковые клетки отличаются от здоровых клеток. Чем больше они различаются, тем быстрее и агрессивнее растет рак. Эксперты называют это степенью дифференциации или градуировки. Оценка предоставляет врачам важную информацию для лечения.
Влияют ли гормоны на рост рака? Женские половые гормоны способствуют росту определенных раковых клеток в груди. В лаборатории специалисты могут выяснить, есть ли у раковых клеток специфические места связывания, так называемые рецепторы, для этих гормонов. Если это так, то это гормон-рецептор-положительный рак молочной железы. Для этого эксперты используют аббревиатуру HR+. В этом случае рост рака можно замедлить с помощью так называемой антигормональной терапии. Примерно у 80 из 100 женщин с раком молочной железы это HR+. Если рак не чувствителен к гормонам, его называют гормонально-негативным раком молочной железы (HR-).
Магнитно-резонансная томография (МРТ)
Магнитно-резонансная томография ( МРТ ) не является стандартным тестом для выявления рака молочной железы. Это вариант, например, если врачи не могут с уверенностью определить, рак ли это молочной железы, несмотря на маммографию, УЗИ и биопсию. Ложноположительные результаты при МРТ легче получить, чем при других визуализирующих исследованиях. Это означает, что результаты МРТ указывают на рак молочной железы, даже если у пострадавшего человека на самом деле нет рака. Это может, например, привести к ненужному беспокойству или ненужной биопсии.
Если подозрение на рак молочной железы подтвердится, врачи в некоторых случаях назначат дополнительные обследования. К ним относятся, среди прочего:
- Маммография другой груди
- УЗИ другой груди
- МРТ молочных желез
- Рентген легких
- Сцинтиграфия костей
- Ультразвуковое исследование печени и других органов
- КТ или МРТ грудной клетки и брюшной полости
Результаты этих исследований дают врачам информацию о том, распространился ли рак на другую грудь, другие ткани или органы. Они относят отдельные результаты к определенной схеме: так называемой классификации TNM . Используя эту классификацию, специалисты могут оценить, насколько далеко рак распространился на область вокруг груди и образовались ли метастазы. Это позволяет врачам определить, какое лечение наиболее подходит, и оценить прогноз.
Лечение Рака молочной железы
Как оперируют рак молочной железы? Операция в операционной.
Сегодня хирургическое вмешательство по-прежнему необходимо для лечения злокачественных опухолей молочной железы. В большинстве случаев можно обойтись без радикального удаления молочной железы , провести операцию более щадяще и сохранить грудь.
Операция обычно следует за постановкой диагноза . Однако иногда этому предшествует химиотерапия , антигормональная терапия и/или терапия антителами , чтобы уменьшить или полностью уничтожить опухоль . Целью операции является удаление всех опухолевых клеток из молочной железы. На всякий случай часть окружающих здоровых тканей также удаляется . При последующем гистологическом исследовании края разреза исследуют на предмет наличия в них опухолевых клеток. В противном случае можно предположить, что опухоль полностью удалена.
 Органосохраняющая хирургия
Органосохраняющая хирургия
Органосохраняющие операции не представляют для пациенток более высокого риска рецидива , чем радикальное удаление молочной железы, если опухоль полностью удалена (здоровая ткань на краю разреза при микроскопическом исследовании) и впоследствии облучена грудь.
Возможность проведения органосохраняющей операции зависит от индивидуального характера опухоли :
Опухоль не должна быть слишком большой по отношению к молочной железе и должна быть локализована .
Как правило, кожа груди и мышцы грудной стенки не должны поражаться.
В молочной железе не должно быть других опухолей , расположенных далеко друг от друга.
Никаких дополнительных обширных предраковых поражений быть не должно .
В конечном итоге возможность органосохраняющей операции должна решаться индивидуально для каждого пациента на основании визуализации, патологических характеристик и клинического обследования.
Удаление груди – мастэктомия
Лишь у некоторых пациенток приходится удалять всю молочную железу : молочную железу, кожу и покровный слой грудной мышцы (фасцию) . Однако во многих случаях удается сохранить кожу (так называемая «кожосберегающая» или кожосохраняющая мастэктомия), а в некоторых случаях и сосок (так называемая «сосохраняющая» мастэктомия). Мастэктомия необходима, если:
- опухоль слишком большая
- опухоли растут в нескольких отдаленных местах
- поражается кожа груди
- предраковые поражения присутствуют по всей молочной железе .
- опухоль не удалось полностью удалить во время предыдущей операции , а последующая операция с сохранением молочной железы невозможна или если лучевая терапия невозможна (например, если вы очень стары),
- если рак молочной железы воспалительный («воспалительный рак молочной железы») или по желанию пациента.
Хотя мышцы груди также были удалены много лет назад, сегодня используется более щадящая форма мастэктомии, при которой эти мышцы сохраняются. Это означает, что основание груди сохраняет свой круглый контур.
Особенно перед мастэктомией, а также во время крупных операций по сохранению груди пациенты должны узнать о различных вариантах реконструкции груди еще до операции , поскольку первые меры по реконструкции груди могут быть проведены уже во время процедуры. Мастэктомия с сохранением кожи предполагает немедленную реконструкцию путем замены удаленной молочной железы силиконовым имплантатом.
Удаление лимфатических узлов
Когда клетки рака молочной железы метастазируют , то есть когда они распространяются из молочной железы по всему телу, это обычно сначала происходит через лимфатическую систему . Лимфатические каналы от груди впадают в лимфатические узлы подмышками. Если раньше эти лимфатические узлы всегда удалялись во время операции (« подмышечная диссекция »), то теперь стандартной практикой является удаление только так называемых сторожевых лимфатических узлов – первых, которые лежат в лимфатической системе между грудью и подмышкой . Однако это возможно только в том случае, если до операции лимфатические узлы выглядели нормальными.
Если при последующем гистологическом исследовании дозорных не обнаружено раковых клеток, можно предположить, что опухоль еще не распространилась и, следовательно, нет метастазов в другие лимфатические узлы или другие части тела. Если во время или после операции выяснится, что поражено более двух сторожевых лимфатических узлов , обычно приходится удалять не менее десяти лимфатических узлов . Однако если поражено максимум два лимфатических узла, дальнейшего удаления можно избежать, если после операции провести лучевую терапию и дальнейшее лечение. Лишь в некоторых случаях (крупные, пальпируемые метастазы в лимфатические узлы или те, которые заметны при визуализации) требуется удаление более десяти лимфатических узлов.
Если операции планируется предшествовать медикаментозной терапией (« неоадъювантной »), то после неоадъювантного лечения сторожевые лимфатические узлы следует удалить и обследовать во избежание обширной операции на подмышечной впадине, если сторожевые лимфатические узлы отрицательные, т.е. в норме.
Хирургия метастатического рака молочной железы
Поскольку при наличии отдаленных метастазов заболевание уже невозможно вылечить , хирургического вмешательства на опухоли молочной железы часто избегают и вместо этого используют только системную медикаментозную терапию . В некоторых случаях удаление опухоли все еще может быть полезным, особенно при метастазах в костях , после успешного медикаментозного лечения. Хирургическое вмешательство также может быть целесообразным, если есть местные опухолевые осложнения . Радиация также может помочь .
Антигормональная терапия рака молочной железы
Какая гормональная терапия подойдет? Около двух третей всех злокачественных опухолей молочной железы растут в зависимости от женских половых гормонов, особенно эстрогена. Они в большом количестве вырабатываются в яичниках от менархе – наступления половой зрелости – до менопаузы – отсутствия менструации. Но другие ткани также производят эстроген.
После того, как стала известна связь между раком молочной железы и действием гормонов , многим женщинам удалили яичники (овариэктомия) или подвергли облучению. Однако возникающее в результате бесплодие было очень проблематичным для молодых пациентов. Антигормональная терапия (также: «эндокринная терапия »), доступная с 1970-х годов, останавливает или замедляет рост опухоли с помощью лекарств. После лечения менструации часто возобновляются; фертильность можно сохранить.
Патолог использует образцы тканей, полученные при биопсии или операции, чтобы определить статус рецепторов гормонов (HR) опухолевых клеток. HR-позитивные опухоли чувствительны к эстрогену и/или прогестерону и поэтому их рост можно остановить с помощью антигормональной терапии.
Как и химиотерапия, антигормональная терапия также действует по всему организму (« системная терапия ») и, следовательно, борется даже с самыми маленькими опухолями, которые еще невозможно обнаружить с помощью доступных сегодня вариантов. Это может увеличить скорость выздоровления на 30 процентов. Этот положительный эффект сохраняется в течение 10 лет после прекращения терапии. Однако важно, чтобы лечение продолжалось как минимум пять-десять лет . Поэтому даже при возникновении побочных эффектов лечение не следует немедленно прекращать , а врач должен проконсультировать вас о том, как можно лечить нежелательные симптомы. Преимущество антигормональной терапии перед химиотерапией : здоровые клетки не подвергаются непосредственному воздействию, хотя прекращение гормонального эффекта все равно на них влияет. В целом антигормоны лучше переносятся и их можно принимать в течение многих лет.
Когда дело доходит до эндокринной терапии, различают антиэстрогены , которые предотвращают передачу сигнала роста непосредственно к гормональным рецепторам опухолевых клеток, и активные ингредиенты, которые ингибируют выработку гормонов - как в жировой, так и в мышечной ткани. (ингибиторы ароматазы) или в яичниках аналоги ГнРГ (ГнРГ означает гонадотропин-рилизинг гормоны). Тип антигормонального лечения зависит, прежде всего, от того, находится ли пациентка до (пре-) или после (пост-)менопаузы. Женщин в период менопаузы обычно рассматривают как пациенток в пременопаузе.
Антиэстрогены блокируют рецепторы раковых клеток
Гормональная терапия антиэстрогенами, такими как тамоксифен , не останавливает выработку эстрогена , но блокирует действие эстрогена на опухолевые клетки . Антиэстрогены занимают места связывания рецепторов гормонов на опухолевых клетках, к которым в противном случае стыкуются эстрогены и запускают стимул роста. Если рецептор блокируется таким образом, эстроген больше не может связываться и, следовательно, не может развивать свое действие. Дальнейшим развитием является фулвестрант, антагонист рецепторов эстрогена . Он также захватывает рецепторы эстрогена раковых клеток, но полностью их отключает, в то время как тамоксифен, который используется уже давно, остается активным. Фулвестрант также вызывает разрушение рецепторов. Фулвестрант в настоящее время одобрен только для пациентов с распространенным или метастатическим раком молочной железы .
Использование тамоксифена при раке молочной железы
Ингибитор эстрогеновых рецепторов тамоксифен применяется до и после менопаузы. После операции – при адъювантной, дополнительной терапии – снижает риск возврата заболевания ( рецидива ). При метастатических опухолях прогрессирование заболевания замедляется.
Фулвестрант в настоящее время используется только у женщин, у которых рак молочной железы прогрессировал и/или метастазировал.
Тамоксифен - принимают по таблетке один раз в день (обычно 20 мг), а фулвестрант вводят в мышцу в виде инъекции (500 мг) один раз в месяц после трехкратного введения в начале терапии с интервалом в две недели. В каждую половину ягодицы вводят по 250 мг.
Побочные эффекты. Терапия тамоксифеном может быть связана с симптомами менопаузы : приливы, потливость, тошнота, нарушения сна, проблемы с концентрацией внимания, депрессивные настроения, вагинальные кровотечения, вагинальный зуд, а также тромбозы и психологические нарушения. Побочные эффекты фулвестранта аналогичны, но менее выражены. Остаточный эстрогенный эффект тамоксифена может также привести к избыточной слизистой оболочке матки (гиперплазии эндометрия) и, реже, к раку эндометрия . У пожилых женщин хрусталики глаз также могут помутнеть (катаракта).
 Антигормональная терапия в сочетании с химиотерапией или лучевой терапией.
Антигормональная терапия в сочетании с химиотерапией или лучевой терапией.
Если пациенты принимают антигормональную терапию в дополнение к адъювантной химиотерапии , антигормональную терапию начинают после завершения химиотерапии. Если проводится лучевая терапия , одновременно можно начать антигормональное лечение. У женщин в пременопаузе, у которых функция яичников сохранена после химиотерапии, хорошую эффективность показало сочетание эндокринной терапии (тамоксифен или ингибиторы ароматазы) с подавлением функции яичников, особенно у женщин моложе 35 лет.
Как долго длится антигормональная терапия?
Адъювантная антигормональная терапия первоначально проводится в течение пяти лет . Однако исследования показали, что еще пять лет эндокринной терапии еще больше снижают риск рецидива . Поэтому врач должен уточнить у пациента, следует ли или можно ли продолжать лечение через пять лет. Это следует делать с учетом индивидуального риска рецидива, возникших побочных эффектов и пожеланий пациента. Можно рассмотреть возможность перехода на другую эндокринную терапию. Выбор формы терапии должен также учитывать текущий менопаузальный статус пациентки.
В случае метастатического рака молочной железы лечение продолжают до прогрессирования заболевания. При необходимости антигормональное лечение можно продолжить с использованием другого действующего вещества или эндокринную терапию можно комбинировать с таргетной терапией .
Борьба с побочными эффектами
По сравнению с химиотерапией антигормональная терапия обычно считается хорошо переносимой. Тем не менее, побочные эффекты и здесь могут оказаться стрессовыми – тем более, что лечение длится долгие годы. Недостаток гормонов обычно приводит к таким симптомам менопаузы , как приливы, потливость, выпадение волос и сухость слизистых оболочек, в том числе в области влагалища. Ингибиторы ароматазы также могут вызывать проблемы с суставами и мышцами и увеличивать риск остеопороза . Вот почему рекомендуется регулярное измерение плотности костной ткани, предпочтительно с помощью сканирования DXA (двухэнергетическая рентгеновская абсорбциометрия).
Побочные эффекты антигормональной терапии обычно можно облегчить с помощью здорового питания , занятий спортом и физических упражнений . Сопутствующие лекарства также могут эффективно бороться с ним. Однако важно, чтобы не использовались гормональные препараты или действующие вещества , способные снизить эффективность антигормональной терапии (в том числе зверобоя, соевых продуктов, антидепрессантов). Поэтому использование всех лекарств и травяных сборов следует обсудить с лечащим врачом.
Спорт или другие физические нагрузки, здоровое питание с большим количеством кальция и витамина D могут предотвратить остеопороз во время антигормональной терапии. Для пациентов, у которых уже имеется низкая плотность костной ткани («остеопения») до начала гормональной терапии, может быть полезным профилактическое применение бисфосфонатов или антител деносумаба.
Нужна ли мне дополнительная контрацепция во время антигормональной терапии?
Антигормональная терапия не заменяет контрацепцию у женщин до наступления менопаузы . Однако гормональные контрацептивы, такие как противозачаточные таблетки, бесполезны при раке молочной железы. Использование медной ВМС возможно, при этом гормональные ВМС не следует заменять. Если у вас уже есть гормональная ВМС, переход на медьсодержащую ВМС следует обсудить с вашим гинекологом.
Рак молочной железы - лучевая терапия. Как действует лучевая терапия при раке молочной железы?
Помимо хирургического вмешательства и медикаментозного лечения, лучевая терапия или лучевая терапия являются наиболее часто используемой формой терапии для женщин с раком молочной железы. Высокие дозы ионизирующего излучения (например, рентгеновских лучей) повреждают генетический материал облученных клеток – как здоровых, так и оставшихся раковых клеток. Однако раковые клетки не имеют столь хорошо функционирующих систем восстановления, как нормальные клетки. Именно поэтому повреждения , вызванные радиацией, не могут быть устранены – клетка погибает.
Для кого применяется лучевая терапия?
Лучевая терапия используется после операции, то есть в качестве адъюванта, для разрушения опухолевых клеток, которые, возможно, не были удалены, и таким образом предотвращения рецидива. После органосохраняющей операции облучение всей оставшейся молочной железы в настоящее время является стандартной практикой, поскольку это может значительно снизить вероятность возвращения (рецидива) рака молочной железы. В отдельных случаях низкого риска - если пациентка старше 70 лет, имеет небольшую опухоль, HR-положительную и HER2-отрицательную, без поражения лимфатических узлов и она также получает эндокринную терапию - можно обойтись без лучевой терапии.
После мастэктомии лучевая терапия часто не требуется . Облучение проводят только при очень больших опухолях, если опухоль не удалось полностью удалить, несмотря на эту операцию, если существует повышенный риск рецидива или если поражено более трех лимфатических узлов. Если поражено от одного до трех подмышечных лимфатических узлов, но риск опухоли низкий, можно обойтись без лучевой терапии грудной стенки.
В редких случаях — если риск рецидива невелик — достаточно частичного облучения молочной железы , при котором облучается только часть молочной железы, содержащая опухоль. Это можно сделать во время операции или через несколько дней после нее.
Первичная или единственная лучевая терапия (без операции) используется только в том случае, если операция не может быть проведена (например, если опухоль неоперабельна или из-за тяжелых сопутствующих заболеваний) или если пациент отказывается от операции.
Если в лимфатических узлах подмышечной впадины обнаружены метастазы , но лимфатические узлы не очищены или остатки опухоли остались в подмышечной впадине, облучают также станции лимфатических узлов - в зависимости от находок в подмышечной впадине, от ключицы или, очень редко, в области вокруг грудины. Лимфатические дренажные пути также облучаются, если доказано поражение лимфатических узлов. Если поражена подмышка, необходимость в этом будет оцениваться индивидуально.
В запущенных случаях лучевая терапия также используется для лечения метастазов. Здесь, в отличие от адъювантной лучевой терапии, лучевая терапия больше не используется для лечения, а скорее для облегчения таких симптомов, как боль.
Рак молочной железы - химиотерапия
Химиотерапия часто связана с неизлечимыми заболеваниями. Это неправильно. Химиотерапию применяют не только при запущенных опухолях, но и на ранних стадиях (неоадъювантная, т.е. до операции, или адъювантная, т.е. после операции), если есть соответствующие показания. Цель состоит в том, чтобы уничтожить крошечные опухолевые отложения, так называемые микрометастазы , в других органах. Поскольку их существование не может быть доказано с помощью современных методов визуализации и, следовательно, не может быть надежно исключено, пациентам с соответствующей группой риска рекомендуется «превентивная» химиотерапия. Это может заметно снизить риск рецидива и смерти .
Для кого применяется химиотерапия?
Только пациенты с ранним раком молочной железы и доказанным низким риском рецидива могут быть избавлены от химиотерапии. Это особенно касается гормонально-положительных и HER2 -отрицательных пациентов без поражения лимфатических узлов, для которых достаточно чисто эндокринной терапии . Курсы биомаркеров и генетические тесты могут помочь достоверно идентифицировать эту группу пациентов.
Профилактическая химиотерапия теперь рекомендуется всем остальным пациентам с раком молочной железы на ранней стадии , независимо от их возраста:
Пациентки с гормонально-позитивным, HER2-негативным раком молочной железы и высоким риском рецидива (например, поражением более трех лимфатических узлов, высокой степенью дегенерации и т. д.) сначала получают химиотерапию, а затем антигормональную терапию. Здесь рекомендуется так называемая плотнодозная, т. е. усиленная, терапия.
Пациентки с HER2-положительным раком молочной железы получают химиотерапию в сочетании с терапией антителами, направленными против HER2, с трастузумабом (и, возможно, пертузумабом) . Системное лечение также можно провести или начать до операции ( неоадъювантное ). Если эти пациенты относятся к группе высокого риска и терапия уже является неоадъювантной , в дополнение к трастузумабу назначают дополнительное антитело, нацеленное на HER2 . Пациентки с тройным негативным раком молочной железы (гормональный рецептор и HER2-отрицательный) также получают химиотерапию, которую при необходимости можно назначать неоадъювантно. Здесь также рекомендуется высокодозная химиотерапия . Терапию дополняют ингибитором контрольных точек пембролизумабом до и после операции .
Таргетная терапия рака молочной железы
Таргетная терапия рака — это молекулярно -биологический подход к лечению пациентов с раком. Хотя химиотерапия имеет достаточно неспецифический эффект и повреждает также здоровые клетки, новые специфические активные ингредиенты («биологические препараты») могут более точно атаковать раковые клетки – эффективный метод, который обычно менее стрессоустойчив для всего организма.
Таргетная терапия, используемая в настоящее время при раке молочной железы, направлена против веществ-посредников («лигандов») , блокирует места связывания рецепторов этих веществ-посредников на поверхности клеток или ингибирует сигнальные пути внутри клеток и, таким образом, влияет на рост опухоли или кровеносных сосудов. Новые иммунотерапевтические препараты также входят в число целевых активных ингредиентов , поскольку они связываются с конкретными «контрольными точками» иммунного ответа и тем самым стимулируют его . В последние годы разработка таргетных активных ингредиентов была очень динамичной. Следующие терапевтические агенты одобрены фармацевтическими органами для лечения рака молочной железы — некоторые в излечимом случае, другие — только в неизлечимом, т. е. метастатическом:
Ингибирование роста клеток посредством блокады рецепторов с использованием антител HER2 (трастузумаб, пертузумаб)
Ингибирование роста клеток цитостатиками/химиотерапевтическими средствами, которые связаны с антителами HER2 (трастузумаб эмтанзин [T-DM1], трастузумаб дерукстекан ) или антителами TROP2 (сацитузумаб говитекан) в так называемых конъюгатах антитело-лекарственное средство.
- Ингибирование роста клеток путем нарушения передачи сигнала с помощью ингибиторов тирозинкиназы (лапатиниб, нератиниб, тукатиниб)
- Ингибирование роста клеток из-за нарушения сигнального пути mTOR ингибиторами mTOR (эверолимус )
- Ингибирование роста клеток за счет ингибирования киназы CDK4/6 ингибиторами CDK4/6 (палбоциклиб, абемациклиб, рибоциклиб)
- Ингибирование роста сосудов ( ингибирование ангиогенеза ) с использованием антител VEGF (бевацизумаб)
- Ингибирование роста клеток за счет нарушения передачи сигнала через PI3-киназу (алпелисиб)
- Гибель клеток вследствие нарушения восстановления поврежденной ДНК путем ингибирования фермента репарации PARP (олапариб, талазопариб).
- Активация иммунной системы против опухолевых клеток путем связывания антител с иммунными контрольными точками (атезолизумаб, пембролизумаб).
- Кроме того, многие другие таргетные подходы находятся в разработке и проверяются на предмет их эффективности в клинических исследованиях.
Терапия метастазов
Когда опухолевые клетки мигрируют по лимфатическим сосудам или крови в другие органы и размножаются там, образуются дочерние опухоли, так называемые метастазы . Клетки рака молочной железы могут колонизироваться практически во всех органах тела; рак молочной железы чаще всего метастазирует в скелет, легкие и печень и реже в мозг.
Метастатический рак молочной железы обычно лечат системно, т.е. с помощью лекарств, поскольку системная терапия действует по всему организму и направлена на воздействие на все рассеянные раковые клетки. Какое лечение (эндокринное, химиотерапевтическое ) с таргетной терапией или без нее, бисфосфонатами или ингибиторами RANK-лиганда (денозумаб) использовать при наличии костных метастазов, определяется биологией опухоли и локализацией метастазов (см. 8.4). Если возможно, перед выбором лечения следует заново определить свойства метастазов, поскольку они иногда отличаются от свойств исходной опухоли.
Некоторые метастазы также можно лечить локально .
При кожных метастазах можно применять местную химиотерапию с использованием крема. Существует также вариант электрохимиотерапии, т.е. применения химиотерапии в сочетании с электролечением метастазов в коже. В первую очередь это используется для контроля метастазов. Увеличение продолжительности жизни еще не доказано.
Особым видом местной химиотерапии является внутрибрюшинная химиотерапия.Цитостатический раствор вводится в брюшную полость с целью борьбы с перитонеальными метастазами (карцинозом брюшины) непосредственно на месте. Однако это не используется при раке молочной железы.
Хирургическое лечение может использоваться в очень специфических ситуациях при метастазах в кожу, кости, печень, легкие и мозг , а также для лечения скопления жидкости в грудной клетке (плевральный выпот). Однако в целом медикаментозная терапия здесь имеет приоритет.
Облучение возможно при метастазах в кожу, кости, мягкие ткани (мышцы) и головной мозг.
Бисфосфонаты или ингибиторы лиганда RANK (денозумаб) используются для лечения костных метастазов.
Пункции (дренирование жидкости) не борются непосредственно с метастазами, но облегчают симптомы, которые они вызывают: при наличии жидкости в брюшной полости (асцит) в результате поражения брюшины (перитональный рак) или в случае жидкости в грудной клетке (плевральный выпот) в результате поражения легких или плевры (плевральный карциноз). При необходимости пункцию можно сочетать с плевродезом, т. е. медикаментозным сращиванием легкого и плевры.
Примечание: информация из Интернета может дать вам общее представление, однако она не способна заменить консультацию врача.